Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
舟山 知夫; 横田 裕一郎; 鈴木 芳代; 坂下 哲哉; 小林 泰彦
JAEA-Review 2014-050, JAEA Takasaki Annual Report 2013, P. 73, 2015/03
原子力機構・マイクロビーム細胞照射研究グループでは、集束式重イオンマイクロビームを用いた、従来のコリメーション式重イオンマイクロビームを用いた照射より高速でかつ正確な細胞照準照射技術の開発を進めている。これまでに集束式重イオンマイクロビームを用いた細胞の照準照射のための要素技術の開発を行ってきた。そこで、2013年度は、これまでに確立したそれらの要素技術を用いて、実際の細胞への高速で正確な照準照射技術の確立を目指す実験を実施した。実験では、ヒト子宮頸がん細胞由来細胞株HeLaを用い、顕微鏡下で細胞試料へのスキャンビームを用いた照準照射を行った。その結果、CR-39上で検出したイオンヒット位置と、細胞核内に検出された H2AXフォーカスの位置が一致したことから、細胞への高速な照準照射を実現することができたことが確かめられた。
H2AXフォーカスの位置が一致したことから、細胞への高速な照準照射を実現することができたことが確かめられた。
小林 泰彦; 舟山 知夫; 和田 成一; 坂下 哲哉; 柿崎 竹彦; 浜田 信行*; 横田 裕一郎; 古澤 佳也*
KEK Proceedings 2005-5, p.6 - 8, 2005/10
環境ラドン被曝や銀河宇宙線など極低フルエンス率の高LET重イオンによる生物影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、原研・高崎研では、個別の培養細胞に照準して正確な個数の重イオンを照射し、その影響を経時的に観察する実験システムを開発している。今回、照射前に試料を自動スキャンして細胞を検出するオフライン顕微鏡及び取得した座標データに従ってビーム位置に標的細胞を移動するオンライン顕微鏡の各々の試料ステージを更新し、従来は 10
10 m以上の誤差があった試料移動の位置再現精度が
m以上の誤差があった試料移動の位置再現精度が 1
1 mに向上した。これによって、多数の標的細胞を次々に自動照準して連続的にシングルイオン照射することが可能になった。併せて、最近の細胞照射実験の結果についても報告する。
mに向上した。これによって、多数の標的細胞を次々に自動照準して連続的にシングルイオン照射することが可能になった。併せて、最近の細胞照射実験の結果についても報告する。
小林 泰彦; 舟山 知夫; 和田 成一; 古澤 佳也*; 青木 瑞穂*; Shao, C.*; 横田 裕一郎; 坂下 哲哉; 松本 孔貴*; 柿崎 竹彦; et al.
宇宙生物科学, 18(4), p.235 - 240, 2004/12
銀河宇宙線のように、低フルエンス・低フルエンス率の高LET重イオン(粒子線)による生物影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、高エネルギー重イオンマイクロビームを顕微鏡観察下の生物試料に照射するために原研・高崎研・バイオ技術研究室で開発した細胞局部照射装置を用いて、哺乳動物培養細胞を個別に重イオンで照射・観察する実験系を開発した。標的細胞を貫通したイオンのエネルギーと個数をシンチレータ/フォトマルを用いて測定することによって、重イオンを1個ずつカウントしながら正確に照射することが可能となった。さらに、CR-39を直ちに37 Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。国内外の重粒子線のマイクロビーム開発の歴史を概観し、細胞核へのシングルイオンヒット効果やバイスタンダー効果に関する最近の研究成果をレビューする。
Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。国内外の重粒子線のマイクロビーム開発の歴史を概観し、細胞核へのシングルイオンヒット効果やバイスタンダー効果に関する最近の研究成果をレビューする。
小林 泰彦; 舟山 知夫; 和田 成一; 坂下 哲哉
宇宙生物科学, 18(3), p.186 - 187, 2004/11
銀河宇宙線のように、低フルエンス率の高LET重イオン(粒子線)による生物影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、原研・高崎研・バイオ技術研究室で開発した細胞局部照射装置を用いて、哺乳動物培養細胞を個別に重イオンで照射し、その影響を経時的に観察する実験システムを開発している。今回、照射前に試料を自動スキャンして細胞を検出するオフライン顕微鏡及び取得した座標データに従ってビーム位置に標的細胞を移動するオンライン顕微鏡の各々の試料ステージ更新し、従来は 10
10 m以上の誤差があった試料移動の位置再現精度が
m以上の誤差があった試料移動の位置再現精度が 1
1 mに向上したことにより、多数の標的細胞を次々に自動照準して連続的にシングルイオン照射することが可能になった。併せて、最近の細胞照射実験結果について報告する。
mに向上したことにより、多数の標的細胞を次々に自動照準して連続的にシングルイオン照射することが可能になった。併せて、最近の細胞照射実験結果について報告する。
小林 泰彦; 舟山 知夫; 和田 成一*; 田口 光正; 渡辺 宏
Radiation Research, 161(1), p.90 - 91, 2004/01
低線量放射線の生物影響、特に低フルエンス・低フルエンス率の高LET重イオン(粒子線)による影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、高エネルギー重イオンマイクロビームを顕微鏡観察下の生物試料に照射するために原研・高崎研・バイオ技術研究室で開発した細胞局部照射装置を用いて、哺乳動物培養細胞を個別に重イオンで照射・観察する実験系を開発した。標的細胞を貫通したイオンのエネルギーと個数をシンチレータ/フォトマルを用いて測定することによって、重イオンを1個ずつカウントしながら正確に照射することが可能となった。さらに、CR-39を直ちに37 Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。
Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。
小林 泰彦; 舟山 知夫; 和田 成一; 田口 光正; 渡辺 宏
Nuclear Instruments and Methods in Physics Research B, 210(1-4), p.308 - 311, 2003/09
重イオンマイクロビームは、放射線の生物作用研究のための新しいツールとして極めて有望である。原研・高崎研では、銀河宇宙線のような極低フルエンス高LET重粒子線の生物影響の解明、特にトラック構造の局所的エネルギー付与分布による影響をダイレクトに解析することを目指して、サイクロトロンから得られる比較的高エネルギーの重イオンマイクロビームを用いて哺乳動物培養細胞を個別に照射・観察する実験系を開発した。その結果、ArやNeなどの重イオン1個のヒットで細胞の増殖が強く抑制されることを見いだした。
渡辺 宏
Isotope News, 0(8), p.8 - 10, 1994/08
本年3月に製作が完了し、現在調整運転を行っているマイクロビーム細胞照射装置の概要と、本装置を用いて行うことを計画している研究内容について紹介した。
舟山 知夫; 横田 裕一郎; 坂下 哲哉; 鈴木 芳代; 小林 泰彦
no journal, ,
マイクロビーム細胞照射研究グループは、重イオンマイクロビーム生物照射システムの開発と、それを用いた細胞一つ一つに正確に制御したイオンを照射する技術の確立を進めてきた。これまで、サイクロトロンの重イオンビームを四連四重極磁気レンズで集束したビームスポットを顕微鏡下で正確に検出し、スポット位置に細胞を電動ステージで移動することで細胞照準を行ってきたが、この手法を用いる限り、細胞照射のスループットの向上には機械的な限界が伴う。そこで、集束ビームをビームスキャナで高速走査することで、細胞一つ一つに正確かつ高速に重イオンを照射する技術の確立を試みた。CR-39フィルム上に播種したHeLa細胞を生体蛍光染色し、その蛍光画像における位置情報を画像解析で抽出、得られた座標値を元にビームスキャナへの印加電圧を算出し、これを用いて試料への高速走査照射を行った。高速走査照射を行った細胞位置と、CR-39上に可視化したエッチピット位置が合致したこと、および当該細胞への H2AXのフォーカス生成が確認できたことから、照準した細胞への正確な照射を集束ビームの高速走査技術を用いて行うことが可能となったことが確認できた。
H2AXのフォーカス生成が確認できたことから、照準した細胞への正確な照射を集束ビームの高速走査技術を用いて行うことが可能となったことが確認できた。
池田 裕子; 横田 裕一郎; 舟山 知夫; 金井 達明*; 中野 隆史*; 小林 泰彦
no journal, ,
本研究では、ヒト胎児肺由来の正常線維芽細胞株WI-38と、ヒト肺がん細胞H1299/wt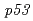 を用いた。炭素線ブロードビーム照射(LET=108keV/
を用いた。炭素線ブロードビーム照射(LET=108keV/ m)した細胞と非照射細胞を非接触で共培養した後、コロニー形成実験を行い、非照射細胞の生存率を測定した。炭素線0.13Gy照射したWI-38と非照射H1299/wt
m)した細胞と非照射細胞を非接触で共培養した後、コロニー形成実験を行い、非照射細胞の生存率を測定した。炭素線0.13Gy照射したWI-38と非照射H1299/wt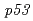 を共培養すると、非照射がん細胞の相対的な生存率が、共培養開始から6時間および24時間後に約15%
を共培養すると、非照射がん細胞の相対的な生存率が、共培養開始から6時間および24時間後に約15% 20%増加した。0.5Gy照射したWI-38を用いた場合では、非照射がん細胞の相対的な生存率が約10%
20%増加した。0.5Gy照射したWI-38を用いた場合では、非照射がん細胞の相対的な生存率が約10% 15%低下することが分かった。また、Carboxy-PTIOを添加した培養液を用いた場合には、共培養開始から6時間および24時間後に、0.5Gy照射群において、非照射がん細胞の相対的な生存率が増加傾向を示した。この結果から、異細胞種間バイスタンダー効果では非照射細胞の生存率低下に、一酸化窒素ラジカルの媒介が関与する可能性が高いが、その一方で相対的な生存率を増加させるシグナルの関与も示唆された。
15%低下することが分かった。また、Carboxy-PTIOを添加した培養液を用いた場合には、共培養開始から6時間および24時間後に、0.5Gy照射群において、非照射がん細胞の相対的な生存率が増加傾向を示した。この結果から、異細胞種間バイスタンダー効果では非照射細胞の生存率低下に、一酸化窒素ラジカルの媒介が関与する可能性が高いが、その一方で相対的な生存率を増加させるシグナルの関与も示唆された。
舟山 知夫; 横田 裕一郎; 坂下 哲哉; 鈴木 芳代; 小林 泰彦
no journal, ,
原子力機構・高崎の集束式重イオンマイクロビーム装置は、TIARAのAVFサイクロトロンで加速された重イオンビームを最小径1 mに集束することができる。このシステムを用いて、ヒト頸がん由来細胞株HeLaへの照準照射実験を実施した。CellTracker Orangeで染色したHeLa細胞をイオン飛跡検出器CR39上に播種し、その位置を蛍光顕微鏡像を画像解析することで抽出した。得られた細胞位置情報を元に、ビームスキャナへの印加電圧を開発したソフトウェアを用いて算出し、細胞にマイクロビームの走査照射を行った。照射後、イオンヒット位置をCR39上のエッチピットとして、細胞に生成したDNA二重鎖切断位置を
mに集束することができる。このシステムを用いて、ヒト頸がん由来細胞株HeLaへの照準照射実験を実施した。CellTracker Orangeで染色したHeLa細胞をイオン飛跡検出器CR39上に播種し、その位置を蛍光顕微鏡像を画像解析することで抽出した。得られた細胞位置情報を元に、ビームスキャナへの印加電圧を開発したソフトウェアを用いて算出し、細胞にマイクロビームの走査照射を行った。照射後、イオンヒット位置をCR39上のエッチピットとして、細胞に生成したDNA二重鎖切断位置を -H2AXのフォーカスとして可視化したところ、両者の位置が一致していることを確認した。この結果から、これらの実験で用いたシステムの構成機器、ソフトウェアコードおよび細胞照射プロトコルが細胞の高速で正確なマイクロビーム照射を実現できる性能を有することが示唆された。
-H2AXのフォーカスとして可視化したところ、両者の位置が一致していることを確認した。この結果から、これらの実験で用いたシステムの構成機器、ソフトウェアコードおよび細胞照射プロトコルが細胞の高速で正確なマイクロビーム照射を実現できる性能を有することが示唆された。
舟山 知夫; 横田 裕一郎; 坂下 哲哉; 鈴木 芳代; 池田 裕子; 小林 泰彦
no journal, ,
原子力機構高崎量子応用研究所では、重イオンの生物照射効果を解析するために、コリメーション式および集束式の2つの重イオンマイクロビームシステムを開発・運用してきた。コリメーション式重イオンマイクロビームシステムでは、これまでに培養細胞のみならず、線虫やカイコ、メダカなどの生物個体も含めた多様な生物試料への照準照射を実施し、その重イオン照射効果の測定や、バイスタンダー効果の機構解析、さらには、マイクロビームをラジオサージェリーツールとして用いた個体における発生学・生理学的な解析実験を実施してきた。一方の、集束式重イオンマイクロビームシステムは、コリメーション式重イオンマイクロビームでは実現が難しい高精度かつ高速な照準照射を実現するために開発された。これまでに、このシステムを用いてスキャンビームを用いたヒト培養細胞への高速照準照射技術を開発した。
村田 和俊*; 野田 真永*; 尾池 貴洋*; 高橋 昭久*; 吉田 由香里*; 鈴木 義行*; 大野 達也*; 舟山 知夫; 小林 泰彦; 高橋 健夫*; et al.
no journal, ,
本研究では、Rho情報伝達経路を介したヒト肺がん細胞A549株の細胞遊走能に炭素イオン照射が及ぼす影響を明らかにすることを研究の目的とした。細胞遊走能の定量はwound-healingアッセイを、細胞表面突起の形成の評価はFアクチン染色を用いた。細胞生存率はWST-1アッセイを用いて定量し、MLC2タンパク質の発現量および同タンパクセリン19残基のリン酸化量の定量にはウエスタンハイブリダイゼーション法を用いた。炭素イオン照射したA549細胞における照射効果をこれらの方法で解析した結果、炭素イオン照射が、A549細胞の遊走能をRho情報伝達経路を介して増加させる一方で、Rho結合キナーゼ阻害剤によりその照射効果が抑制されることが明らかになった。
神長 輝一; 篠田 航平; 福岡 壮太郎; 中上 裕貴; 横谷 明徳
no journal, ,
Fucci化されたHeLa細胞を試料として用い、X線照射による細胞周期遅延をライブセル観察により調べた。KEK放射光施設(PF)のBL27Bから得られるX線マイクロビームを利用し、顕微鏡下で細胞に照射した。本顕微照射システムでは、長時間に渡る細胞の継時観察が困難である。このため照射後細胞をビームラインから外し、培養器を備えた別の顕微鏡システムにセットした。オンラインとオフラインの二つの顕微システムにおいて照射細胞の位置座標を共有するため、新たに位置調整用フィルムアタッチメントを製作した。数十個のHeLa-Fucci細胞からなるマイクロコロニー中心部に60 60
60 mのX線マイクロビームを照射し、72時間タイムラプス観察を行った。その結果、照射細胞に細胞周期遅延や細胞死、細胞融合などの影響が観察されたことに加え、非照射細胞にも細胞周期遅延が線量や細胞周期に依存して起こることを見出した。これは、新しいタイプのバイスタンダー効果であると考えられる。
mのX線マイクロビームを照射し、72時間タイムラプス観察を行った。その結果、照射細胞に細胞周期遅延や細胞死、細胞融合などの影響が観察されたことに加え、非照射細胞にも細胞周期遅延が線量や細胞周期に依存して起こることを見出した。これは、新しいタイプのバイスタンダー効果であると考えられる。